INSTITUCIONAL
legislação
O Departamento de Ciência e Tecnologia embasa os seus processos de trabalho em diversas normas e legislações. Suas diretrizes norteadoras são:
Política Nacional de Ciência, Tecnologia e Inovação em Saúde (PNCTIS)
Integrante da Política Nacional de Saúde, formulada no âmbito do Sistema Único de Saúde (SUS). O artigo 200, inciso V, da Constituição Federal estabelece as competências do SUS e, dentre elas, inclui o incremento do desenvolvimento científico e tecnológico em sua área de atuação.
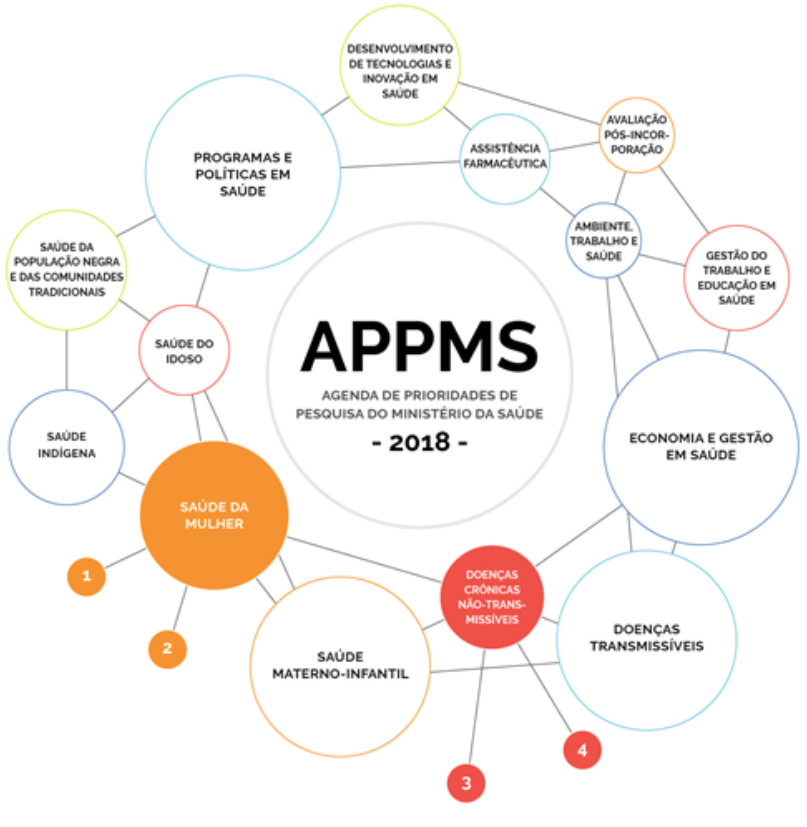
Agenda de Prioridades de Pesquisa do Ministério da Saúde (APPMS)
Identifica demandas de pesquisa que possam subsidiar a formulação de políticas públicas e à tomada de decisão de gestores do SUS. Foi elaborada em um processo de priorização de temas conjuntamente com todas as secretarias do Ministério da Saúde.
Consulte as demais normativas que o Departamento de Ciência e Tecnologia
Artigo 200 Constituição Federal de 1988, inciso V
“incrementar, em sua área de atuação, o desenvolvimento científico e tecnológico e a inovação”. A Constituição prevê ainda a articulação, coordenação e cooperação entre entes públicos e privados, com vistas a promover o desenvolvimento científico, tecnológico e a inovação (Art. 219 A e B). (https://www.senado.leg.br/atividade/const/con1988/con1988_14.12.2017/art_200_.asp)
Lei Orgânica da Saúde, nº 8.080, de 19 de setembro de 1990
define a competência de articular políticas e programas de saúde e de CT&I no campo de atuação do SUS. (http://www.planalto.gov.br/ccivil_03/leis/l8080.htm)
Decreto nº 9.795, de 17 de maio de 2019
que aprova a Estrutura Regimental e o Quadro Demonstrativo dos Cargos em Comissão e das Funções de Confiança do Ministério da Saúde. (http://www.planalto.gov.br/ccivil_03/_ato2019-2022/2019/decreto/D9795.htm)
Marco Legal da Ciência, Tecnologia e Inovação
que altera nove leis, prevê o aprimoramento de medidas de incentivo à inovação e à pesquisa científica e tecnológica, por meio da Lei nº. 13.243, de 11 de janeiro de 2016. (http://www.planalto.gov.br/ccivil_03/_Ato2015-2018/2016/Lei/L13243.htm)
Decreto nº 9.283, de 7 de fevereiro de 2018
que fortalece as competências do Departamento de Ciência e Tecnologia. (https://www2.camara.leg.br/legin/fed/decret/2018/decreto-9283-7-fevereiro-2018-786162-norma-pe.html)
Lei nº 13.709, de 14 de agosto de 2018
que dispõe sobre a proteção de dados pessoais e altera a Lei nº 12.965, de 23 de abril de 2014 (Marco Civil da Internet). (http://www.planalto.gov.br/ccivil_03/_Ato2015-2018/2018/Lei/L13709.htm)
Lei nº 12.527, de 18 de novembro de 2011
Lei de acesso à informação. (http://www.planalto.gov.br/ccivil_03/_ato2011-2014/2011/lei/l12527.htm)
Decreto 7.724, de 16 de maio de 2012
Decreto de acesso à informação. (http://www.planalto.gov.br/ccivil_03/_ato2011-2014/2012/decreto/d7724.htm)
Decreto nº 9.203, de 22 de novembro de 2017
Política de Governança da administração pública (http://www.planalto.gov.br/ccivil_03/_ato2015-2018/2017/decreto/D9203.htm)
Decreto nº 9.203, de 22 de novembro de 2017
Política de Governança da administração pública (http://www.planalto.gov.br/ccivil_03/_ato2015-2018/2017/decreto/D9203.htm)
Ações Estratégicas em Pesquisa Clínica
Portaria nº 559, de 9 de março de 2018
que institui do Plano de Ação de Pesquisa Clínica no Brasil. (http://bvsms.saude.gov.br/bvs/saudelegis/gm/2018/prt0559_14_03_2018.html)
RDC nº 9, de 20 de fevereiro de 2015
que dispõe sobre o regulamento para a realização de ensaios clínicos com medicamentos no Brasil. (http://portal.anvisa.gov.br/documents/10181/3503972/RDC_09_2015_.pdf/843a88bd-3381-489e-8711-aca256cb4360)
RDC nº 10, de 20 de fevereiro de 2015
que dispõe sobre o regulamento para a realização de ensaios clínicos com dispositivos médicos no Brasil. (http://portal.anvisa.gov.br/documents/10181/3503972/RDC_09_2015_.pdf/843a88bd-3381-489e-8711-aca256cb4360)
RDC nº 172, de 8 de setembro de 2017
que dispõe sobre os procedimentos para a importação e a exportação de bens e produtos destinados à pesquisa científica ou tecnológica e à pesquisa envolvendo seres humanos, e dá outras providências. (http://portal.anvisa.gov.br/documents/10181/2917036/RDC_172_2017_.pdf/433b3940-65fe-4dfd-b4d5-9962f4b94626)
RDC nº 204, de 27 de dezembro de 2017
que dispõe sobre o enquadramento na categoria prioritária de petições de registro, pós-registro e anuência prévia em pesquisa clínica de medicamentos. (http://portal.anvisa.gov.br/documents/10181/2718376/RDC_204_2017_.pdf/b2d4ae64-2d91-44e9-ad67-b883c752c094)
RDC nº 205, de 28 de dezembro de 2017
que estabelece procedimento especial para anuência de ensaios clínicos, certificação de boas práticas de fabricação e registro de novos medicamentos para tratamento, diagnóstico ou prevenção de doenças raras. (http://portal.anvisa.gov.br/documents/10181/2718376/RDC_205_2017_.pdf/996fc46e-216b-44ab-b8c8-2778151b786e)
RDC nº 208, de 05 de janeiro de 2018
que dispõe sobre a simplificação de procedimentos para a importação de bens e produtos sujeitos à Vigilância Sanitária. (http://portal.anvisa.gov.br/documents/10181/2957335/RDC_208_2018_.pdf/eccf9152-9aae-43d0-83b4-e2f6b3015425)
RDC nº 214, de 07 de fevereiro de 2018
que dispõe sobre as boas práticas em células humanas para uso terapêutico e pesquisa clínica. (http://portal.anvisa.gov.br/documents/10181/3078078/(1)RDC_214_2018_.pdf/8acbc5cb-bca6-4725-b9de-da584e3c024a)
RDC nº 260, de 21 de dezembro de 2018
que dispõe sobre as regras para a realização de ensaios clínicos com produto de terapia avançada investigacional no Brasil. (http://portal.anvisa.gov.br/documents/10181/2718376/RDC_260_2018_.pdf/dd889184-bd4a-40ea-ae1c-b93155b20ea1)
Instrução normativa n° 20, de 2 de outubro de 2017
que dispõe sobre procedimentos de inspeção em Boas Práticas Clínicas para ensaios clínicos com medicamentos. (http://www.lex.com.br/legis_27520728_INSTRUCAO_NORMATIVA_N_20_DE_2_DE_OUTUBRO_DE_2017.aspx)
Documento das Américas: Boas Práticas Clínicas (Versão 1.1)
Ética em Pesquisa
Declaração Universal de Bioética e Direitos Humanos
Portaria nº 559, de 9 de março de 2018
institui o Plano de Ação de Pesquisa Clínica no Brasil. (http://bvsms.saude.gov.br/bvs/saudelegis/gm/2018/prt0559_14_03_2018.html)
Lei nº 13.243, de 11 de janeiro de 2016
que dispõe sobre estímulos ao desenvolvimento científico, à pesquisa, à capacitação científica e tecnológica e à inovação, nos termos da Emenda Constitucional nº 85, de 26 de fevereiro de 2015. (http://www.planalto.gov.br/ccivil_03/_Ato2015-2018/2016/Lei/L13243.htm)
Portaria de Consolidação nº 3/GM/MS, de 28 de setembro de 2017
que institui a Rede Nacional de Pesquisa Clínica – RNPC (http://bvsms.saude.gov.br/bvs/saudelegis/gm/2017/prc0003_03_10_2017.html)
RDC da Anvisa nº 09 e 10, de 20 de fevereiro de 2015
que dispõe sobre o regulamento para a realização de ensaios clínicos com medicamentos no Brasil (http://portal.anvisa.gov.br/documents/10181/3503972/RDC_09_2015_.pdf/843a88bd-3381-489e-8711-aca256cb4360)
Resolução nº 466, de 12 de dezembro de 2012
do Conselho Nacional de Saúde – CNS, que aprova as diretrizes e normas regulamentadoras de pesquisas envolvendo seres humanos e dispõe sobre as atribuições da Comissão Nacional de Ética em Pesquisa – Conep e dos Comitês de Ética em Pesquisa – CEP; (http://bvsms.saude.gov.br/bvs/saudelegis/cns/2013/res0466_12_12_2012.html)
Norma Operacional CNS nº 001/2013
que dispõe sobre a organização e funcionamento do Sistema CEP/CONEP, e estabelece que a Secretaria de Ciência, Tecnologia e Insumos Estratégicos do Ministério da Saúde – SCTIE/MS exerce a função de Secretaria Executiva da CONEP/CNS (http://andromeda.ensp.fiocruz.br/etica/sites/default/files/documentos/CNS%20%20Norma%20Operacional%20001.pdf)
Resolução 466 do Conselho Nacional de Saúde, de 12 de dezembro de 2012
que aprova as normas regulamentadoras de pesquisas envolvendo seres humanos. (http://bvsms.saude.gov.br/bvs/saudelegis/cns/2013/res0466_12_12_2012.html)
Resolução 441 do Conselho Nacional de Saúde, de 12 de maio de 2011
que trata sobre armazenamento de material biológico humano. (https://conselho.saude.gov.br/resolucoes/2011/Reso441.pdf)
Resolução 446 do Conselho Nacional de Saúde, de 11 de agosto de 2011
que trata da composição da Comissão Nacional de Ética em Pesquisa. (https://conselho.saude.gov.br/resolucoes/2011/Reso446.DOC)
Resolução 346 do Conselho Nacional de Saúde, de 13 de janeiro de 2005
que trata da regulamentação para tramitação de projetos de pesquisa multicêntricos no sistema Comitês de Ética em Pesquisa-CEP. (http://bvsms.saude.gov.br/bvs/saudelegis/cns/2005/res0346_13_01_2005.html)
Resolução 304 do Conselho Nacional de Saúde, de 09 de agosto de 2000
que aprova as normas para Pesquisas Envolvendo Seres Humanos sobre Povos Indígenas.(https://conselho.saude.gov.br/resolucoes/2000/Reso304.doc)
Resolução 340 do Conselho Nacional de Saúde, de 08 de julho de 2004
que aprova as diretrizes para análise ética e tramitação dos projetos de pesquisa da área temática especial de genética humana. (http://bvsms.saude.gov.br/bvs/saudelegis/cns/2004/res0340_08_07_2004.html)
Resolução 292 do Conselho Nacional de Saúde, de 08 de julho de 1999
que trata de definições e normas de pesquisas coordenadas do exterior ou com participação estrangeira e pesquisas que envolvam remessa de material biológico para o exterior. (http://bvsms.saude.gov.br/bvs/saudelegis/cns/1999/res0292_08_07_1999.html)
Resolução 251 do Conselho Nacional de Saúde, de 07 de agosto de 1997
sobre pesquisa com novos fármacos, medicamentos, vacinas e testes diagnósticos. (http://bvsms.saude.gov.br/bvs/saudelegis/cns/1997/res0251_07_08_1997.html)
Resolução 370 do Conselho Nacional de Saúde, de 08 de março de 2007
sobre o registro e credenciamento e renovação de registro e credenciamento dos CEPs institucionais. (http://bvsms.saude.gov.br/bvs/saudelegis/cns/2007/res0370_08_03_2007.html)
Resolução 301 do Conselho Nacional de Saúde, de 16 de março de 2000
sobre as modificações da Declaração de Helsinque.(https://conselho.saude.gov.br/resolucoes/2000/Reso301.doc)
Resolução 240 do Conselho Nacional de Saúde, de 05 de junho de 1997
que define representação de usuários nos CEPs. (http://andromeda.ensp.fiocruz.br/etica/sites/default/files/documentos/Res%20240_1997.pdf)
Resolução 506 do Conselho Nacional de Saúde, de 03 de fevereiro de 2016
sobre o processo de acreditação de CEP. (https://conselho.saude.gov.br/resolucoes/2016/Reso_506.pdf)
Resolução 510 do Conselho Nacional de Saúde , de 07 de abril de 2016
sobre as normas aplicáveis a pesquisas em ciências humanas e sociais (http://bvsms.saude.gov.br/bvs/saudelegis/cns/2016/res0510_07_04_2016.html)
Resolução 563 do Conselho Nacional de Saúde, de 10 de novembro de 2017
que aprova as diretrizes para atenção integral às pessoas com doenças raras no âmbito do Sistema Único de Saúde (SUS) e institui incentivos financeiros de custeio (https://conselho.saude.gov.br/resolucoes/2017/Reso563.pdf)
Resolução 580 do Conselho Nacional de Saúde, de 22 de março de 2018
que regulamenta o disposto no item XIII.4 da Resolução CNS nº 466, de 12 de dezembro de 2012, que estabelece que as especificidades éticas das pesquisas de interesse estratégico para o Sistema Único de Saúde (SUS) serão contempladas em Resolução específica, e dá outras providências. (https://conselho.saude.gov.br/resolucoes/2018/Reso580.pdf)
Coordenação de Gestão de Programas de Pesquisa
Normas regulamentadoras do Programa de Apoio ao Desenvolvimento Institucional do Sistema Único de Saúde (PROADI-SUS)
Lei nº 12.101, de 27 de novembro de 2009
que dispõe sobre a certificação das entidades beneficentes de assistência social; regula os procedimentos de isenção de contribuições para a seguridade social.
(http://www.planalto.gov.br/ccivil_03/_ato2007-2010/2009/lei/l12101.htm)
Portaria de Consolidação n.º 05, de 28 de setembro de 2017, anexo XCIII (páginas 534 a 548)
rege o Programa de Apoio ao Desenvolvimento Institucional do Sistema Único de Saúde.
Normas regulamentadoras do Programa Nacional de Apoio à Atenção Oncológica (PRONON) e do Programa Nacional de Apoio à Atenção da Saúde da Pessoa com Deficiência (PRONAS/PCD)
Decreto n° 7.988, de 17 de abril de 2013
que regulamenta os programas Programa Nacional de Apoio à Atenção Oncológica (PRONON) e Programa Nacional de Apoio à Atenção da Saúde da Pessoa com Deficiência (PRONAS/PCD).
(http://www.planalto.gov.br/ccivil_03/_ato2011-2014/2013/decreto/d7988.htm)
Lei n° 12.715, de 17 de setembro de 2012
institui o PRONON e PRONAS/PCD.
(http://www.planalto.gov.br/ccivil_03/_ato2011-2014/2012/lei/l12715.htm);
Portaria de Consolidação n° 05, de 28 de setembro de 2017
rege o PRONON e do PRONAS/PCD.
(http://bvsms.saude.gov.br/bvs/saudelegis/gm/2017/prc0005_03_10_2017.html)

Maecenas eu placerat ante. Fusce ut neque justo, aliquet enim. In hac habitasse platea aumst. Nullam commodo au erat.
© 2019 Todos os direitos reservados
MAPA DO SITE
ONDE ESTAMOS
